įŁļŖ│ž║═ļŖĮŌ│ž
1Ż«įŁļŖ│ž║═ļŖĮŌ│žĄ─▒╚▌^Ż║
|
čbų├ |
įŁļŖ│ž |
ļŖĮŌ│ž |
|
īŹ└² |
||
|
įŁ└Ē |
╩╣č§╗»▀ĆįŁĘ┤æ¬ųąļŖūėū„Č©Ž“ęŲäėŻ¼Å─Č°ą╬│╔ļŖ┴„ĪŻ▀@ĘN░č╗»īW─▄▐Dūā?y©Łu)ķļŖ─▄Ą─čbų├Įąū÷įŁļŖ│žĪŻ |
╩╣ļŖ┴„═©▀^ļŖĮŌ┘|╚▄ę║Č°į┌ĻÄĪóĻ¢ā╔śOę²Ųč§╗»▀ĆįŁĘ┤æ¬Ą─▀^│╠Įąū÷ļŖĮŌĪŻ▀@ĘN░čļŖ─▄▐Dūā?y©Łu)ķ╗»īW─▄Ą─čbų├Įąū÷ļŖĮŌ│žĪŻ |
|
ą╬│╔Śl╝■ |
ó┘ļŖśOŻ║ā╔ĘN▓╗═¼Ą─ī¦¾wŽÓ▀BŻ╗ ó┌ļŖĮŌ┘|╚▄ę║Ż║─▄┼cļŖśOĘ┤æ¬ĪŻ |
ó┘ļŖį┤Ż╗ ó┌ļŖśOŻ©ČĶąį╗“ĘŪČĶąįŻ®Ż╗ ó█ļŖĮŌ┘|Ż©╦«╚▄ę║╗“╚█╗»æB(t©żi)Ż®ĪŻ |
|
Ę┤æ¬ŅÉą═ |
ūį░l(f©Ī)Ą─č§╗»▀ĆįŁĘ┤æ¬ |
ĘŪūį░l(f©Ī)Ą─č§╗»▀ĆįŁĘ┤æ¬ |
|
ļŖśO├¹ĘQ |
ė╔ļŖśO▒Š╔Ēąį┘|øQČ©Ż║ š²śOŻ║▓─┴Žąį┘|▌^▓╗╗ŅØŖĄ─ļŖśOŻ╗ žōśOŻ║▓─┴Žąį┘|▌^╗ŅØŖĄ─ļŖśOĪŻ |
ė╔═ŌļŖį┤øQČ©Ż║ Ļ¢śOŻ║▀BļŖį┤Ą─š²śOŻ╗ ĻÄśOŻ║▀BļŖį┤Ą─žōśOŻ╗ |
|
ļŖśOĘ┤æ¬ |
žōśOŻ║Zn-2e-=Zn2+ Ż©č§╗»Ę┤æ¬Ż® š²śOŻ║2H++2e-=H2Ī³Ż©▀ĆįŁĘ┤æ¬Ż® |
ĻÄśOŻ║Cu2+ +2e- = Cu Ż©▀ĆįŁĘ┤æ¬Ż® Ļ¢śOŻ║2Cl--2e-=Cl2Ī³ Ż©č§╗»Ę┤æ¬Ż® |
|
ļŖūė┴„Ž“ |
žōśOĪ·š²śO |
ļŖį┤žōśOĪ·ĻÄśOŻ╗Ļ¢śOĪ·ļŖį┤š²śO |
|
ļŖ┴„ĘĮŽ“ |
š²śOĪ·žōśO |
ļŖį┤š²śOĪ·Ļ¢śOŻ╗ĻÄśOĪ·ļŖį┤žōśO |
|
─▄┴┐▐D╗» |
╗»īW─▄Ī·ļŖ─▄ |
ļŖ─▄Ī·╗»īW─▄ |
|
æ¬ė├ |
ó┘┐╣Įī┘Ą─ļŖ╗»Ė»╬gŻ╗ ó┌īŹė├ļŖ│žĪŻ |
ó┘ļŖĮŌ╩│¹}╦«Ż©┬╚ēA╣żśI(y©©)Ż®Ż╗ó┌ļŖÕāŻ©ÕāŃ~Ż®Ż╗ó█ļŖę▒Ż©ę▒¤ÆNaĪóMgĪóAlŻ®Ż╗ó▄Š½¤ÆŻ©Š½Ń~Ż®ĪŻ |
2Ż«╗»īWĖ»╬g║═ļŖ╗»Ė»╬gĄ─ģ^(q©▒)äe
|
╗»īWĖ»╬g |
ļŖ╗»Ė»╬g | |
|
ę╗░ŃŚl╝■ |
Įī┘ų▒Įė║═ÅŖč§╗»ä®Įėė| |
▓╗╝āĮī┘Ż¼▒Ē├µ│▒ر |
|
Ę┤æ¬▀^│╠ |
č§╗»▀ĆįŁĘ┤æ¬Ż¼▓╗ą╬│╔įŁļŖ│žĪŻ |
ę“įŁļŖ│žĘ┤æ¬Č°Ė»╬g |
|
ėą¤oļŖ┴„ |
¤oļŖ┴„«a╔· |
ėąļŖ┴„«a╔· |
|
Ę┤æ¬╦┘┬╩ |
ļŖ╗»Ė»╬gŻŠ╗»īWĖ»╬g | |
|
ĮY╣¹ |
╩╣Įī┘Ė»╬g |
╩╣▌^╗ŅØŖĄ─Įī┘Ė»╬g |
3Ż«╬³č§Ė»╬g║═╬÷ÜõĖ»╬gĄ─ģ^(q©▒)äe
|
ļŖ╗»Ė»╬gŅÉą═ |
╬³č§Ė»╬g |
╬÷ÜõĖ»╬g |
|
Śl╝■ |
╦«─ż╦ßąį║▄╚§╗“│╩ųąąį |
╦«─ż╦ßąį▌^ÅŖ |
|
š²śOĘ┤æ¬ |
O2 + 4e- + 2H2O == 4OH- |
2H+ + 2e-==H2Ī³ |
|
žōśOĘ┤æ¬ |
Fe ŻŁ2e-==Fe2+ |
Fe ŻŁ2e-==Fe2+ |
|
Ė»╬gū„ė├ |
╩Ūų„ꬥ─Ė»╬gŅÉą═Ż¼Š▀ėąÅVĘ║ąį |
░l(f©Ī)╔·į┌─│ą®Šų▓┐ģ^(q©▒)ė“ā╚ |
4Ż«ļŖĮŌĪóļŖļx║═ļŖÕāĄ─ģ^(q©▒)äe
|
ļŖĮŌ |
ļŖļx |
ļŖÕā | |
|
Śl╝■ |
╩▄ų▒┴„ļŖū„ė├ |
╩▄¤ß╗“╦«Ęųūėū„ė├ |
╩▄ų▒┴„ļŖū„ė├ |
|
īŹ┘| |
ĻÄĻ¢ļxūėČ©Ž“ęŲäėŻ¼į┌ā╔śO░l(f©Ī)╔·č§╗»▀ĆįŁĘ┤æ¬ |
ĻÄĻ¢ļxūėūįė╔ęŲäėŻ¼¤o├„’@Ą─╗»īWūā╗» |
ė├ļŖĮŌĄ─ĘĮĘ©į┌Įī┘▒Ē├µÕā╔Žę╗īėĮī┘╗“║ŽĮ |
|
īŹ└² |
CuCl2 ļŖĮŌ==== CuŻ½Cl2 |
CuCl2==Cu2++2ClĪź |
Ļ¢śO Cu ŻŁ2e- = Cu2+ ĻÄśO Cu2++2e- = Cu |
|
ĻPŽĄ |
Ž╚ļŖļx║¾ļŖĮŌŻ¼ļŖÕā╩ŪļŖĮŌĄ─æ¬ė├ | ||
5Ż«ļŖÕāŃ~Ī󊽤ÆŃ~▒╚▌^
|
ļŖÕāŃ~ |
Š½¤ÆŃ~ | |
|
ą╬│╔Śl╝■ |
ÕāīėĮī┘ū„Ļ¢śOŻ¼Õā╝■ū„ĻÄśOŻ¼ļŖÕāę║▒žĒÜ║¼ėąÕāīėĮī┘Ą─ļxūė |
┤ųŃ~Įī┘ū„Ļ¢śOŻ¼Š½Ń~ū„ĻÄśOŻ¼CuSO4╚▄ę║ū„ļŖĮŌę║ |
|
ļŖśOĘ┤æ¬ |
Ļ¢śO Cu ŻŁ2e- = Cu2+ ĻÄśO Cu2++2e- = Cu |
Ļ¢śOŻ║Zn - 2e- = Zn2+ Cu - 2e- = Cu2+ Ą╚ ĻÄśOŻ║Cu2+ + 2e- = Cu |
|
╚▄ę║ūā╗» |
ļŖÕāę║Ą─ØŌČ╚▓╗ūā |
╚▄ę║ųą╚▄┘|ØŌČ╚£pąĪ |
6Ż«ļŖĮŌĘĮ│╠╩ĮĄ─īŹ└²Ż©ė├ČĶąįļŖśOļŖĮŌŻ®Ż║
|
ļŖĮŌ┘|╚▄ę║ |
Ļ¢śOĘ┤æ¬╩Į |
ĻÄśOĘ┤æ¬╩Į |
┐éĘ┤æ¬ĘĮ│╠╩Į Ż©Śl╝■Ż║ļŖĮŌŻ® |
╚▄ę║╦ßēAąįūā╗» |
|
CuCl2 |
2Cl--2e-=Cl2Ī³ |
Cu2+ +2e-= Cu |
CuCl2= Cu +Cl2Ī³ |
Ī¬Ī¬ |
|
HCl |
2Cl--2e-=Cl2Ī³ |
2H++2e-=H2Ī³ |
2HCl=H2Ī³+Cl2Ī³ |
╦ßąį£p╚§ |
|
Na2SO4 |
4OH--4e-=2H2O+O2Ī³ |
2H++2e-=H2Ī³ |
2H2O=2H2Ī³+O2Ī³ |
▓╗ūā |
|
H2SO4 |
4OH--4e-=2H2O+O2Ī³ |
2H++2e-=H2Ī³ |
2H2O=2H2Ī³+O2Ī³ |
Ž¹║─╦«Ż¼╦ßąįį÷ÅŖ |
|
NaOH |
4OH--4e-=2H2O+O2Ī³ |
2H++2e-=H2Ī³ |
2H2O=2H2Ī³+O2Ī³ |
Ž¹║─╦«Ż¼ēAąįį÷ÅŖ |
|
NaCl |
2Cl--2e-=Cl2Ī³ |
2H++2e-=H2Ī³ |
2NaCl+2H2O=H2Ī³+Cl2Ī³+2NaOH |
H+Ę┼ļŖŻ¼ēAąįį÷ÅŖ |
|
CuSO4 |
4OH--4e-=2H2O+O2Ī³ |
Cu2+ +2e-= Cu |
2CuSO4+2H2O=2Cu+ O2Ī³+2H2SO4 |
OHĪź Ę┼ļŖ,╦ßąįį÷ÅŖ |
┐╝³cĮŌšf
1Ż«ļŖ╗»Ė»╬gŻ║░l(f©Ī)╔·įŁļŖ│žĘ┤æ¬Ż¼ėąļŖ┴„«a╔·
Ż©1Ż®╬³č§Ė»╬g
žōśOŻ║FeŻŁ2e-==Fe2+
š²śOŻ║O2+4e-+2H2O==4OH-
┐é╩ĮŻ║2Fe+O2+2H2O==2Fe(OH)2
4Fe(OH)2+O2+2H2O==4Fe(OH)3 2Fe(OH)3==Fe2O3+3H2O
Ż©2Ż®╬÷ÜõĖ»╬gŻ║ CO2+H2OH2CO3H++HCO3-
žōśOŻ║Fe ŻŁ2e-==Fe2+
š²śOŻ║2H+ + 2e-==H2Ī³
┐é╩ĮŻ║Fe + 2CO2 + 2H2O = Fe(HCO3)2+ H2Ī³
Fe(HCO3)2╦«ĮŌĪó┐šÜŌč§╗»Īó’L┤Ą╚šĢ±Ą├Fe2O3ĪŻ
2Ż«Įī┘Ą─Ę└ūo
ó┼Ė─ūāĮī┘Ą─ā╚▓┐ĮM┐ŚĮYśŗĪŻ║ŽĮõōųą║¼ėą║ŽĮį¬╦žŻ¼╩╣ĮM┐ŚĮYśŗ░l(f©Ī)╔·ūā╗»Ż¼─═Ė»╬gĪŻ╚ńŻ║▓╗õPõōĪŻ
óŲį┌Įī┘▒Ē├µĖ▓╔w▒ŻūoīėĪŻ│ŻęŖĘĮ╩ĮėąŻ║═┐ė═ų¼Īóė═Ųß╗“Ė▓╔w╠┬┤╔Īó╦▄┴ŽĄ╚Ż╗╩╣▒Ē├µ╔·│╔ų┬├▄č§╗»─żŻ╗į┌▒Ē├µÕāę╗īėėąūį╬ę▒Żūoū„ė├Ą─┴Ēę╗ĘNĮī┘ĪŻ
óŪļŖ╗»īW▒ŻūoĘ©
ó┘═Ō╝ėļŖį┤Ą─ĻÄśO▒ŻūoĘ©:Įė╔Ž═Ō╝ėų▒┴„ļŖį┤śŗ│╔ļŖĮŌ│žŻ¼▒╗▒ŻūoĄ─Įī┘ū„ĻÄśOĪŻ
ó┌Ā▐╔³Ļ¢śOĄ─ĻÄśO▒ŻūoĘ©Ż║═Ō╝ėžōśO▓─┴ŽŻ¼śŗ│╔įŁļŖ│žŻ¼▒╗▒ŻūoĄ─Įī┘ū„š²śO
3ĪŻ│ŻęŖīŹė├ļŖ│žĄ─ĘNŅÉ║═╠ž³c
ó┼Ė╔ļŖ│žŻ©ī┘ė┌ę╗┤╬ļŖ│žŻ®
ó┘ĮYśŗŻ║õ\═▓Īó╠ŅØMMnO2Ą─╩»─½Īó╚▄ėąNH4ClĄ─║²ĀŅ╬’ĪŻ
ó┌ļŖśOĘ┤æ¬ žōśOŻ║Zn-2e-=Zn2+
š²śOŻ║2NH4++2e-=2NH3+H2
NH3║═H2▒╗Zn2Ż½ĪóMnO2╬³╩šŻ║ MnO2+H2=MnO+H2O,Zn2Ż½Ż½4NH3=Zn(NH3)42Ż½
óŲŃUąŅļŖ│žŻ©ī┘ė┌Č■┤╬ļŖ│žĪó┐╔│õļŖļŖ│žŻ®
ó┘ ĮYśŗŻ║ŃU░ÕĪó╠ŅØMPbO2Ą─ŃU░ÕĪóŽĪH2SO4ĪŻ
ó┌A.Ę┼ļŖĘ┤æ¬ žōśOŻ║ Pb-2e-+SO42- = PbSO4
š²śOŻ║ PbO2+2e-+4H+ + SO42- = PbSO4+ 2H2O
B.│õļŖĘ┤æ¬ ĻÄśOŻ║PbSO4 +2e-= Pb+ SO42-
Ļ¢śOŻ║PbSO4-2e- + 2H2O = PbO2 +4H+ + SO42-
┐é╩ĮŻ║
ūóęŌŻ║Ę┼ļŖ║═│õļŖ╩Ū═Ļ╚½ŽÓĘ┤Ą─▀^│╠Ż¼Ę┼ļŖū„įŁļŖ│žŻ¼│õļŖū„ļŖĮŌ│žĪŻļŖśO├¹ĘQ┐┤ļŖūėĄ├╩¦Ż¼ļŖśOĘ┤æ¬╩ĮĄ─Ģ°īæę¬Ū¾┼cļxūėĘĮ│╠╩Įę╗śėŻ¼Ūę╝ėŲüĒæ¬┼c┐éĘ┤æ¬╩ĮŽÓ═¼ĪŻ
óŪõćļŖ│ž
ó┘ ĮYśŗŻ║õćĪó╩»─½Īó╣╠æB(t©żi)ĄŌū„ļŖĮŌ┘|ĪŻ
ó┌ļŖśOĘ┤æ¬ žōśOŻ║ 2Li-2e- = 2Li+
š²śOŻ║ I2 +2e-= 2I- ┐é╩ĮŻ║2Li + I2= 2LiI
ó╚A.Üõč§╚╝┴ŽļŖ│ž
ó┘ ĮYśŗŻ║╩»─½Īó╩»─½ĪóKOH╚▄ę║ĪŻ
ó┌ļŖśOĘ┤æ¬
žōśOŻ║ H2- 2e-+ 2OH- = 2H2O
š²śOŻ║ O2 + 4e- + 2H2O= 4OH-
┐é╩ĮŻ║2H2+O2=2H2O
Ż©Ę┤æ¬▀^│╠ųąø]ėą╗赯¼▓╗╩ŪĘ┼│÷╣Ō║═¤ßŻ¼Č°╩Ū«a╔·ļŖ┴„Ż®
ūóęŌŻ║▀ĆįŁä®į┌žōśO╔ŽĘ┤æ¬Ż¼č§╗»ä®į┌š²śO╔ŽĘ┤æ¬ĪŻĢ°īæļŖśOĘ┤æ¬╩ĮĢr▒žĒÜ┐╝æ]Įķ┘|ģó╝ėĘ┤æ¬Ż©Ž╚│ŻęÄ(gu©®)║¾╔Ņ╚ļŻ®ĪŻ╚¶ŽÓ╗źĘ┤æ¬Ą─╬’┘|╩Ū╚▄ę║Ż¼ätąĶę¬¹}ś“Ż©ā╚čbKClĄ─Łéų¼Ż¼ą╬│╔ķ]║Ž╗ž┬ĘŻ®ĪŻ
BŻ«õXĪó┐šÜŌ╚╝┴ŽļŖ│ž ęįõXĪ¬┐šÜŌĪ¬║Ż╦«ļŖ│ž×ķ─▄į┤Ą─ą┬ą═║Ż╦«ś╦ųŠ¤¶ęččąųŲ│╔╣”ĪŻ▀@ĘN¤¶ęį╚Īų«▓╗▒MĄ─║Ż╦«×ķļŖĮŌ┘|╚▄ę║Ż¼┐┐┐šÜŌųąĄ─č§ÜŌ╩╣õX▓╗öÓč§╗»Č°į┤į┤▓╗öÓ«a╔·ļŖ┴„ĪŻų╗ę¬░褶Ę┼╚ļ║Ż╦«ųąŻ¼öĄ(sh©┤)ĘųńŖ║¾Š═Ģ■░l(f©Ī)│÷ę½č█Ą─ķW╣ŌŻ¼Ųõ─▄┴┐▒╚Ė╔ļŖ│žĖ▀20Ī½50▒ČĪŻ
ļŖśOĘ┤æ¬Ż║õX╩ŪžōśO 4Al-12e-== 4Al3+Ż╗
╩»─½╩Ūš²śO 3O2+6H2O+12e-==12OH-
4Ż«ļŖĮŌĘ┤æ¬ųąĘ┤æ¬╬’Ą─┼ąöÓĪ¬Ī¬Ę┼ļŖĒśą“
ó┼ĻÄśO
A.ĻÄśO▓─┴Ž(Įī┘╗“╩»─½)┐é╩Ū╩▄ĄĮ▒ŻūoĪŻ
B.Ļ¢ļxūėĄ├ļŖūėĒśą“ Ī¬ Įī┘╗ŅäėĒśą“▒ĒĄ─Ę┤▒ĒŻ║
K+ <Ca2+ <Na+ < Mg2+ < Al3+< (H+) < Zn2+< Fe2+ < Sn2+ < Pb2+ < Cu2+< Hg2+ < Ag+
óŲĻ¢śO
A.Ļ¢śO▓─┴Ž╩ŪČĶąįļŖśO(CĪóPtĪóAuĪóTiĄ╚)ĢrŻ║
ĻÄļxūė╩¦ļŖūėŻ║S2- ŻŠ I- ŻŠ Br- ŻŠ Cl- ŻŠ OH- ŻŠ NO3- Ą╚║¼č§╦ßĖ∙ļxūėŻŠF-
B.Ļ¢śO╩Ū╗ŅØŖļŖśOĢrŻ║ļŖśO▒Š╔Ē▒╗č§╗»Ż¼╚▄ę║ųąĄ─ļxūė▓╗Ę┼ļŖĪŻ
5Ż«ļŖĮŌĘ┤æ¬ĘĮ│╠╩ĮĄ─Ģ°īæ▓Į¾EŻ║
ó┘Ęų╬÷ļŖĮŌ┘|╚▄ę║ųą┤µį┌Ą─ļxūėŻ╗
ó┌Ęų╬÷ļxūėĄ─Ę┼ļŖĒśą“Ż╗
ó█┤_Č©ļŖśOĪóīæ│÷ļŖśOĘ┤æ¬╩ĮŻ╗ó▄īæ│÷ļŖĮŌĘĮ│╠╩ĮĪŻ╚ńŻ║
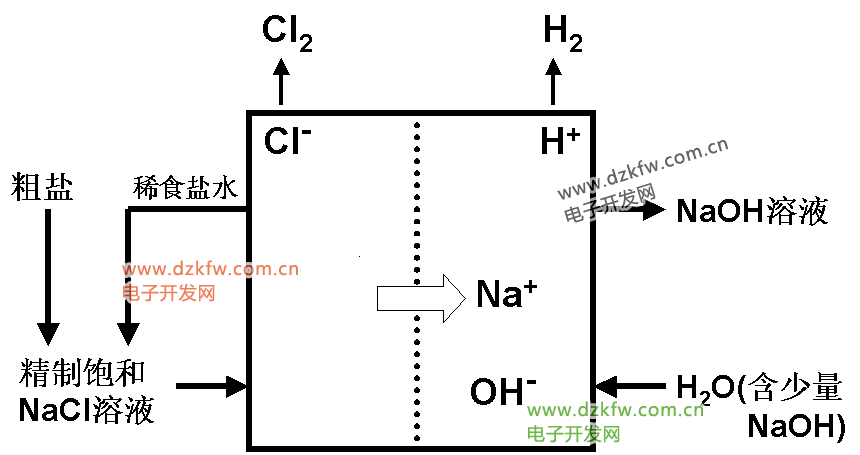
ļŖĮŌNaCl╚▄ę║Ż║2NaCl+2H2O ļŖĮŌ====H2Ī³+Cl2Ī³+2NaOHŻ¼╚▄┘|Īó╚▄䮊∙░l(f©Ī)╔·ļŖĮŌĘ┤æ¬Ż¼PHį÷┤¾
óŲļŖĮŌCuSO4╚▄ę║Ż║2CuSO4 + 2H2OļŖĮŌ====2Cu + O2Ī³+ 2H2SO4
╚▄┘|Īó╚▄䮊∙░l(f©Ī)╔·ļŖĮŌĘ┤æ¬Ż¼ PH£pąĪĪŻ
óŪļŖĮŌCuCl2╚▄ę║Ż║CuCl2ļŖĮŌ==== CuŻ½Cl2Ī³
ļŖĮŌ¹}╦߯║ 2HCl ļŖĮŌ==== H2Ī³Ż½Cl2Ī³
╚▄ä®▓╗ūāŻ¼īŹļH╔Ž╩ŪļŖĮŌ╚▄┘|Ż¼PHį÷┤¾ĪŻ
ó╚ļŖĮŌŽĪH2SO4ĪóNaOH╚▄ę║ĪóNa2SO4╚▄ę║Ż║2H2OļŖĮŌ==== 2H2Ī³ + O2Ī³Ż¼╚▄┘|▓╗ūāŻ¼īŹļH╔Ž╩ŪļŖĮŌ╦«Ż¼PHĘųäe£pąĪĪóį÷┤¾Īó▓╗ūāĪŻ╦ßĪóēAĪó¹}Ą─╝ė╚ļį÷╝ė┴╦╚▄ę║ī¦ļŖąį,Å─Č°╝ė┐ņļŖĮŌ╦┘┬╩Ż©▓╗╩ŪŲ┤▀╗»ū„ė├Ż®ĪŻ
ó╔ļŖĮŌ╚█╚┌NaOH: 4NaOH ļŖĮŌ====4Na + O2Ī³ + H2OĪ³
ó╩ė├Ń~ļŖśOļŖĮŌNa2SO4╚▄ę║: Cu +2H2OļŖĮŌ==== Cu(OH)2 + H2Ī³ Ż©
ūóęŌŻ║▓╗╩ŪļŖĮŌ╦«ĪŻŻ®
6Ż«ļŖĮŌę║Ą─PHūā╗»:Ė∙ō■(j©┤)ļŖĮŌ«a╬’┼ąöÓĪŻ┐┌įEŻ║Ī░ėąÜõ╔·│╔ēAŻ¼ėąč§╔·│╔╦߯╗Č╝ėąØŌČ╚┤¾,Č╝¤oØŌČ╚ąĪĪ▒ĪŻŻ©Ī░ØŌČ╚┤¾Ī▒ĪóĪ░ØŌČ╚ąĪĪ▒╩ŪųĖ╚▄┘|Ą─ØŌČ╚Ż®
7Ż«╩╣ļŖĮŌ║¾Ą─╚▄ę║╗ųÅ═įŁĀŅĄ─ĘĮĘ©Ż║
Ž╚ūī╬÷│÷Ą─«a╬’Ż©ÜŌ¾w╗“│┴ĄĒŻ®ŪĪ║├═Ļ╚½Ę┤æ¬Ż¼į┘īóŲõ╗»║Ž╬’═Č╚ļļŖĮŌ║¾Ą─╚▄ę║ųą╝┤┐╔ĪŻ╚ńŻ║ó┘NaCl╚▄ę║Ż║═©HClÜŌ¾wŻ©▓╗─▄╝ė¹}╦߯®Ż╗ó┌AgNO3╚▄ę║Ż║╝ėAg2O╣╠¾wŻ©▓╗─▄╝ėAgOHŻ®Ż╗ó█CuCl2╚▄ę║Ż║╝ėCuCl2╣╠¾wŻ╗ó▄KNO3╚▄ę║Ż║╝ėH2OŻ╗ó▌CuSO4╚▄ę║Ż║CuOŻ©▓╗─▄╝ėCu2OĪóCu(OH)2ĪóCu2(OH)2CO3Ż®Ą╚ĪŻ
8Ż«ļŖĮŌįŁ└ĒĄ─æ¬ė├
AĪóļŖĮŌ’¢║═╩│¹}╦«Ż©┬╚ēA╣żśI(y©©)Ż®
ó┼Ę┤æ¬įŁ└Ē
Ļ¢śOŻ║ 2Cl- - 2e-== Cl2Ī³
ĻÄśOŻ║ 2H+ + 2e-==H2Ī³
┐éĘ┤æ¬Ż║2NaCl+2H2OļŖĮŌ====H2Ī³+Cl2Ī³+2NaOH
óŲįOéõŻ©Ļ¢ļxūėĮ╗ōQ─żļŖĮŌ▓█Ż®
ó┘ĮM│╔Ż║Ļ¢śOĪ¬TiĪóĻÄśOĪ¬Fe
ó┌Ļ¢ļxūėĮ╗ōQ─żĄ─ū„ė├Ż║╦³ų╗į╩įSĻ¢ļxūė═©▀^Č°ūĶų╣ĻÄļxūė║═ÜŌ¾w═©▀^ĪŻ
óŪųŲ¤²ēA╔·«a▀^│╠Ż©ļxūėĮ╗ōQ─żĘ©Ż®
ó┘╩│¹}╦«Ą─Š½ųŲŻ║┤ų¹}Ż©║¼─Ó╔│ĪóCa2+ĪóMg2+ĪóFe3+ĪóSO42- Ą╚Ż®Ī·╝ė╚ļNaOH╚▄ę║Ī·╝ė╚ļBaCl2╚▄ę║Ī·╝ė╚ļNa2CO3╚▄ę║Ī·▀^×VĪ·╝ė╚ļ¹}╦ßĪ·╝ė╚ļļxūėĮ╗ōQä®(NaR)
ó┌ļŖĮŌ╔·«aų„ę¬▀^│╠Ż©ęŖłD20-1Ż®Ż║NaClÅ─Ļ¢śOģ^(q©▒)╝ė╚ļŻ¼H2OÅ─ĻÄśOģ^(q©▒)╝ė╚ļĪŻĻÄśOH+ Ę┼ļŖŻ¼ŲŲē─┴╦╦«Ą─ļŖļxŲĮ║ŌŻ¼╩╣OH-ØŌČ╚į÷┤¾Ż¼OH-║═Na+ą╬│╔NaOH╚▄ę║ĪŻ
BĪóļŖĮŌę▒¤ÆõX
ó┼įŁ┴ŽŻ║Ż©AŻ®Īó▒∙Š¦╩»Ż║Na3AlF6=3Na++AlF63-
Ż©BŻ®Īóč§╗»õXŻ║õX═┴ĄV
NaAlO2+CO2+2H2O=AlŻ©OHŻ®3Ī²+NaHCO3╗“2NaAlO2+CO2+3H2O=2AlŻ©OHŻ®3Ī²+Na2CO3
Al(OH)3 Ī„Ī¬Ī· Al2O3
2Al2O3═©ļŖĪ·4Al+3O2Ī³
óŲįŁ└Ē
Ļ¢śO 2O2ŻŁŻŁ 4e-=O2Ī³
ĻÄśO Al3Ż½+3e-=Al
┐éĘ┤æ¬Ż║4Al3++6O2ĪźļŖĮŌ====4Al+3O2Ī³
óŪįOéõŻ║ļŖĮŌ▓█Ż©Ļ¢śOCĪóĻÄśOFeŻ®
ę“×ķĻ¢śO▓─┴Ž▓╗öÓĄž┼c╔·│╔Ą─č§ÜŌĘ┤æ¬Ż║C+O2 Ī· CO+CO2Ż¼╣╩ąĶČ©Ģrča│õĪŻ
CĪóļŖÕāŻ║ė├ļŖĮŌĄ─ĘĮĘ©į┌Įī┘▒Ē├µÕā╔Žę╗īėĮī┘╗“║ŽĮĄ─▀^│╠ĪŻ
ó┼ÕāīėĮī┘ū„Ļ¢śOŻ¼Õā╝■ū„ĻÄśOŻ¼ļŖÕāę║▒žĒÜ║¼ėąÕāīėĮī┘Ą─ļxūėĪŻļŖÕāõ\įŁ└ĒŻ║
Ļ¢śO ZnŻŁ2eĪź = Zn2+
ĻÄśO Zn2++2eĪź=Zn
óŲļŖÕāę║Ą─ØŌČ╚į┌ļŖÕā▀^│╠ųą▓╗░l(f©Ī)╔·ūā╗»ĪŻ
óŪį┌ļŖÕā┐žųŲĄ─Śl╝■Ž┬Ż¼╦«ļŖļx│÷üĒĄ─H+║═OHĪźę╗░Ń▓╗ŲĘ┤æ¬ĪŻ
ó╚ļŖÕāę║ųą╝ė░▒╦«╗“ NaCNĄ─įŁę“Ż║╩╣Zn2+ļxūėØŌČ╚║▄ąĪŻ¼Õā╦┘┬²Ż¼Õāīė▓┼─▄ų┬├▄Īó╣Ō┴┴ĪŻ
DĪóļŖĮŌę▒¤Æ╗ŅØŖĮī┘NaĪóMgĪóAlĄ╚ĪŻ
EĪóļŖĮŌŠ½¤ÆŃ~Ż║┤ųŃ~ū„Ļ¢śOŻ¼Š½Ń~ū„ĻÄśOŻ¼ļŖĮŌę║║¼ėąCu2+ĪŻŃ~Ū░Įī┘Ž╚Ę┤æ¬Ą½▓╗╬÷│÷Ż¼Ń~║¾Įī┘▓╗Ę┤æ¬Ż¼ą╬│╔ Ī░Ļ¢śO─ÓĪ▒ĪŻ
üĒį┤Ż║ŠW(w©Żng)ĮjĪŻ▒Š╬─░µÖÓÜwįŁäō(chu©żng)ū„š▀╦∙ėąĪŻ╚¶Ūų┬ō(li©ón)ähĪŻ





 ĘĄ╗žĒö▓┐
ĘĄ╗žĒö▓┐ ╦óą┬Ēō├µ
╦óą┬Ēō├µ Ž┬ĄĮĒōĄū
Ž┬ĄĮĒōĄū